Inleiding
Palliatieve zorg bij patiënten met misselijkheid en/of braken
De multidisciplinaire richtlijn Misselijkheid en braken is een symptoomgebonden richtlijn. De richtlijn geeft adviezen over diagnostiek, voorlichting, preventie en behandeling van misselijkheid en braken bij patiënten in de palliatieve fase en de klachten die daar het gevolg van zijn. De focus van de zorg dient de mens met misselijkheid en/of braken te zijn en niet het symptoom op zichzelf. Dat impliceert het volgende voor de zorg:
- De zorgverlener heeft aandacht voor alle dimensies: dus niet alleen voor de lichamelijke dimensie van misselijkheid en de daardoor veroorzaakte klachten, maar ook voor de psychische, sociale en spirituele/existentiële dimensies. Persisterende misselijkheid kan bijvoorbeeld leiden tot angst rondom het eten, vermijden van sociale activiteiten zoals samen eten. Het hebben van een levensbedreigende ziekte met een beperkt levensperspectief heeft grote gevolgen op al deze gebieden. Zie hiervoor het ‘Kwaliteitskader palliatieve zorg Nederland’ en ‘Algemene principes van palliatieve zorg’.
- De zorgverlener heeft aandacht voor de kernwaarden zoals benoemd in het Kwaliteitskader. Bij deze zorg wordt uitgegaan van in dit kwaliteitskader beschreven principes.
Palliatieve zorg wordt in principe interdisciplinair geleverd. Zorgverleners en vrijwilligers vormen een persoonlijk en dynamisch team in nauwe samenwerking met de patiënt en diens naasten. Waar nodig laten generalistische zorgverleners zich adviseren of ondersteunen door in palliatieve zorg gespecialiseerde zorgverleners. De zorg wordt geleverd op basis van best beschikbare bewijsvoering (evidence-based). Bij gebrek aan bewijs wordt de zorg geleverd op basis van consensus (experience-based). De zorgverlener heeft niet alleen aandacht voor de patiënt, maar ook voor de naasten. Zie hiervoor de themapagina 'Mantelzorgondersteuning in de palliatieve fase' op Palliaweb.
De zorgverlener informeert de patiënt en diens naasten goed en volledig over misselijkheid en braken, de klachten die er het gevolg van (kunnen) zijn, (mogelijke) diagnostiek en (mogelijke) behandeling. Zie hiervoor de module Communicatie en voorlichting. In deze module wordt ook verwezen naar websites waarin adviezen worden gegeven over goede en begrijpelijke communicatie. Voor het brengen van slecht nieuws kan de Handreiking slecht-nieuwsgesprek worden gebruikt.
De zorgverlener beslist samen met de patiënt en de naasten welke diagnostiek en behandeling gewenst, haalbaar en zinvol is (gezamenlijke besluitvorming ofwel ‘shared decision making’). Zie hiervoor de desbetreffende pagina van Palliaweb).
De zorgverlener anticipeert op problemen die zich in de toekomst kunnen voordoen en gaat in gesprek met de patiënt over diens wensen en voorkeuren en passende zorg in de toekomst, mits deze hier open voor staat. Zie hiervoor richtlijn ‘Proactieve zorgplanning’.
Begripsbepaling
Misselijkheid is een subjectieve gewaarwording die moeilijk valt te definiëren. Het is een onaangenaam gevoel in de buik, vaak gepaard gaande met zich ziek voelen, geen zin hebben in eten en (neiging tot) braken.
Plotseling optredende of acute misselijkheid wordt meestal veroorzaakt na directe blootstelling aan een toxine, infectie of stoornis van het centrale zenuwstelsel. Vertraagde misselijkheid treedt op meer dan 24 uur na onder andere chemotherapie. Anticipatoire misselijkheid is een klassieke geconditioneerde reactie op stimuli van zintuigen, herinneringen of emoties die door tijd of plaats geassocieerd zijn met de oorspronkelijke misselijkmakende stimuli. Bijvoorbeeld door het ziekenhuis te zien waar de patiënt chemotherapie heeft toegediend gekregen, kan deze zich misselijk gaan voelen. Wanneer de klachten langer dan 4 weken aanhouden spreken we van chronische misselijkheid. Doorbraakmisselijkheid is een voorbijgaande toename van misselijkheid bij relatief stabiele en voldoende behandelde achtergrond misselijkheid. Refractaire misselijkheid is een misselijkheid die op geen enkele manier verlicht kan worden.
Snelle verzadiging is het optreden van een vol gevoel na het innemen van een kleine hoeveelheid eten of drinken.
Braken is het snel en krachtig retrograad uitstoten van de maaginhoud via de mond. Alhoewel misselijkheid en braken doorgaans worden beschouwd als samen en continu voorkomend, kan misselijkheid zowel onafhankelijk van braken optreden als leiden tot braken, en kan braken soms optreden in de afwezigheid van misselijkheid.
Kokhalzen is een ritmische, actieve samentrekkende beweging van de buikwandspieren in de vorm van heftige oprispingen zonder dat er sprake is van braken.
Regurgitatie is het actief of passief opgeven van de inhoud van de maag in de slokdarm en eventueel in de mond. Dit gaat niet gepaard met misselijkheid.
Prevalentie en prognose
Prevalentiestudies naar symptomatologie in de palliatieve fase worden door meerdere factoren bemoeilijkt. Ten eerste is er een grote verscheidenheid in palliatieve patiënten. Zij kunnen verschillende primaire ziekten in verschillende stadia van ontwikkeling hebben. Tevens kunnen er verschillende ziektebeelden gelijktijdig meespelen. Daarnaast zijn studies vaak in verschillende settings verricht (thuis, verpleeghuis, ziekenhuis, hospice). Tot slot worden misselijkheid en braken vaak tezamen vermeld, maar zijn dit twee symptomen die apart van elkaar kunnen bestaan. Hierdoor is het ingewikkeld de verschillende gerapporteerde prevalentie/incidentie te interpreteren.
Misselijkheid en braken treden op bij respectievelijk 39% en 24% van de patiënten in een vergevorderd stadium van kanker [Teunissen 2007]. Daarnaast treden gebrek aan eetlust (53%) en snelle verzadiging (23%) relatief vaak op. Misselijkheid en braken komen in 30% patiënten met eindstadium nierfalen voor, bij 17-25% bij patiënten met hartfalen en bij 4% van de patiënten met COPD in het laatste jaar voor het overlijden [Solano 2006]. Misselijkheid neemt in prevalentie toe richting het levenseinde, maar wordt juist bij stervende patiënten minder geregistreerd [Mercadante 2000].
De prevalentie is sterk afhankelijk van geslacht, leeftijd, onderliggende ziekte en stadium van de ziekte. Bij patiënten met kanker treden misselijkheid en/of braken vaker op bij vrouwen, op jongere leeftijd en bij een sterke neiging tot wagen- of zeeziekte [Mosa 2020; Sullivan 1983, Tonato 1991, Roila 1987]. Klachten van misselijkheid komen voor bij 10-50% van de patiënten die opioïden gebruiken, vooral in de eerste week van de behandeling of de eerste dagen na het ophogen van de dosering.
Pathofysiologie
Misselijkheid, gevolgd door braken, is een beschermende reflex die wordt uitgelokt door zowel fysieke als psychologische stimuli. Tot de fysieke prikkels behoren onder meer vergiftiging en overmatige uitzetting van de holle ingewanden.
Het neurofysiologische mechanisme dat ten grondslag ligt aan misselijkheid en braken wordt niet uitsluitend gereguleerd door het centrale zenuwstelsel, maar berust ook op een samenspel van verschillende systemen. Misselijkheid wordt voornamelijk gemedieerd via het autonome zenuwstelsel, terwijl braken het gevolg is van activatie van een complex reflexmechanisme waarin diverse neurotransmitters en receptoren betrokken zijn.
Belangrijke neurotransmitters en hun respectievelijke receptoren zijn:
- dopamine (D2-receptor);
- serotonine (5HT2- of 5HT3) (5HT2- of 5HT3-receptor);
- acetylcholine (acetylcholine- of muscarine (M1)-receptor);
- histamine (H1) (H1-receptor);
- substance P (neurokinine-1 of NK1-receptor);
- cannabinoid type 1 (CB1 receptor);
- gamma-aminoboterzuur (GABA) (GABA-receptor).
De voornaamste afferente banen die signalen aanvoeren naar het braakcentrum zijn afkomstig van:
- nervus vagus;
- chemoreceptor triggerzone [gelokaliseerd in de hersenstam (area postrema)];
- evenwichtsorgaan en
- hogere corticale centra.
Perifere stimulatie van chemo- en mechanoreceptoren in maag, darm, lever en peritoneum kan via de nervus vagus leiden tot activatie van het braakcentrum. Dit proces veroorzaakt klinische verschijnselen zoals speekselvloed, bleekheid, zweten, kokhalzen, het beschermend sluiten van de glottis en uiteindelijk braken.
Geneesmiddelen en metabole afwijkingen, zoals hypercalciëmie of nierinsufficiëntie, kunnen het braakcentrum activeren door centrale stimulatie van receptoren in de chemoreceptor triggerzone.
Ook endocriene veranderingen dragen bij aan het ontstaan van misselijkheid en braken. Zo correleren verhoogde vasopressinespiegels met de intensiteit van misselijkheid, waarbij deze spiegels toenemen vóór het ontstaan van braken. Corticotropine-releasing factor activeert remmende motorische zenuwen in het dorsale gebied motorkern van de vagus, wat leidt tot vertraagde maaglediging (gastroparese) en misselijkheid. Deze processen kunnen resulteren in maagdysritmie, een verstoring van de myoelektrische activiteit van de maag. Dit ritme wordt bepaald door de intrinsieke pacemakeractiviteit van de maag, de gladde spiercellen, het enterale en autonome zenuwstelsel en de hormonale invloeden. Zowel een te snelle als een te trage elektrische cadans kan bijdragen aan het ontstaan van misselijkheid.
De psychologische toestand van een patiënt speelt een belangrijke rol in de beleving van misselijkheid en braken. Elke patiënt heeft een unieke drempel voor misselijkheid en braken, die afhankelijk is van de interactie tussen fysiologische en psychologische factoren. Herinneringen, emoties en zintuigelijke waarnemingen kunnen hogere hersencentra activeren, die betrokken zijn bij de regulatie van het braakcentrum (anticipatoire misselijkheid en braken) [Harder 2019]. De interactie tussen deze hersengebieden vormt een plausibele verklaring voor de inter- en intraindividuele variatie in misselijkheidservaringen onder gelijke omstandigheden [Koch 2014, Singh 2016, Stern 2011].
Bij acute misselijkheid komt serotonine vrij, terwijl bij vertraagde misselijkheid de neurotransmitter substance P een centrale rol speelt door binding aan NK1 receptoren. Anticipatoire misselijkheid treedt op vóór toediening van chemotherapie en wordt vaak gekenmerkt door angst. Deze vorm ontstaat door conditionering, waarbij prikkels zoals visuele, olfactorische en cognitieve triggers betrokken zijn. Daarnaast hebben vestibulaire en cerebrale factoren effecten via afferente banen vanuit respectievelijk het evenwichtsorgaan en de cortex cerebri.
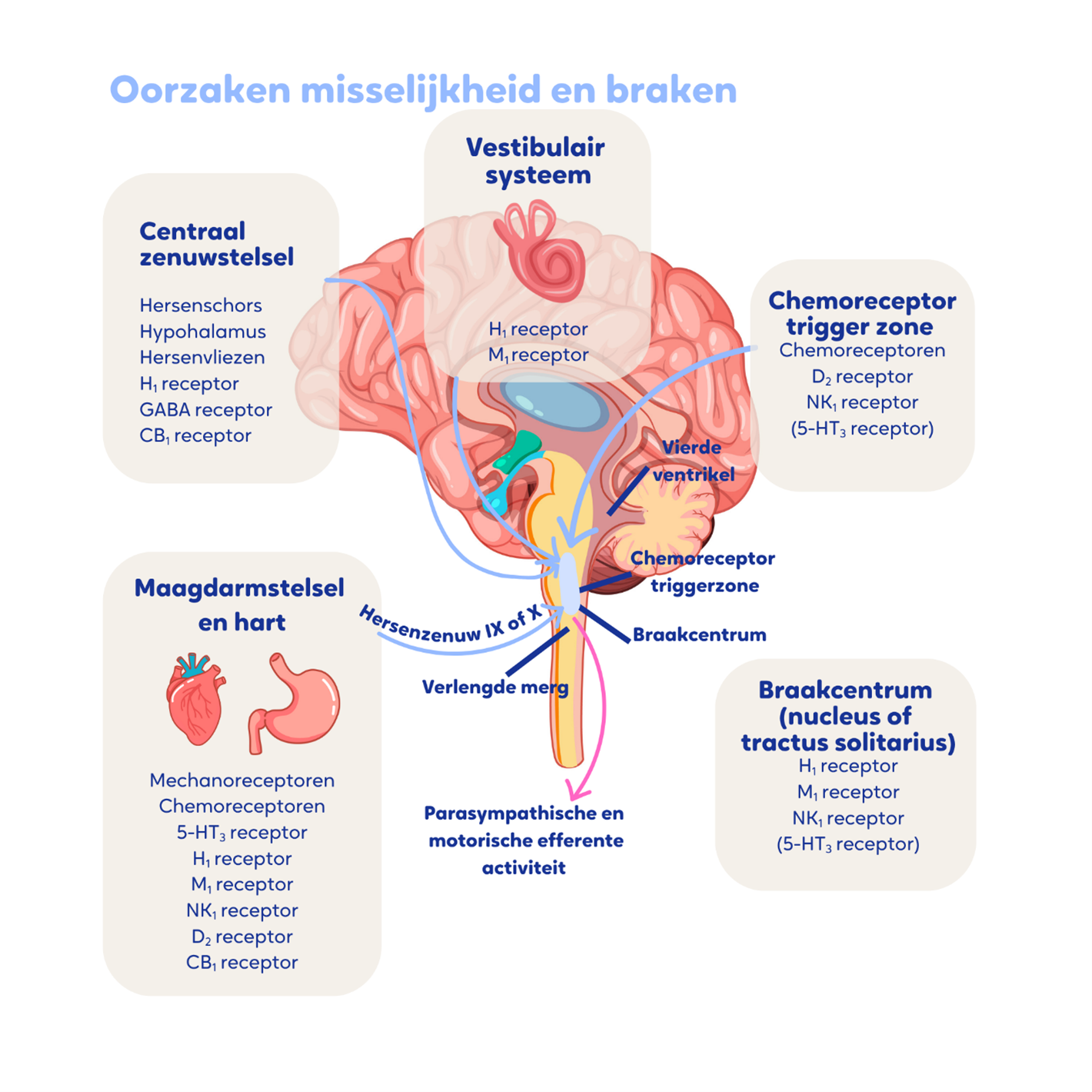
Figuur 1 Neurofysiologische mechanismen van misselijkheid en braken
Het braakcentrum activeert verschillende spiergroepen die betrokken zijn bij het braken. Zo stimuleert het braakcentrum het diafragma via de nervus phrenicus, het dwarsgestreepte spierweefsel van de buikwand en de thorax. Dit verloopt via de spinale zenuwen en het spierweefsel van de maag, slokdarm, larynx en farynx via de nervus vagus. Deze gecoördineerde spieractivatie leidt tot kokhalzen en uiteindelijk tot braken, samen met de bijhorende klinische verschijnselen.
Oorzaken
Er bestaan diverse oorzaken van misselijkheid en/of braken, die vaak gelijktijdig kunnen optreden en elkaar wederzijds versterken. In sommige gevallen zijn er meerdere onderliggende factoren aanwijsbaar, terwijl in andere situaties er geen duidelijke oorzaak vastgesteld kan worden.
De afgifte van serotonine (5-HT3) uit entero-endocriene cellen van het darmepitheel speelt een centrale rol in de inductie van braakreflex. Serotonine activeert 5-HT3-receptoren op afferente vagale banen, wat een belangrijke trigger vormt tot braken. Gastro-intestinale oorzaken van misselijkheid en/of braken kunnen grofweg worden onderverdeeld in acuut (infectie, inflammatie, obstructie) en chronisch (dyspepsie, gastroparese en intestinale pseudo-obstructie).
Vertraagde maaglediging kan het gevolg zijn van verschillende oorzaken: partiële gastrectomie/buismaag, anorexie cachexie syndroom, paraneoplastisch, medicatie (zie ook tabel 1).
Metabole en endocriene ontregelingen kunnen afferente signalen genereren naar de chemoreceptor-triggerzone (CTZ) in de medulla oblongata. Deze zone communiceert met andere structuren in het braakcentrum en kan braken initiëren. Tal van metabole en endocriene aandoeningen kunnen misselijkheid en/of braken veroorzaken, waaronder diabetische ketoacidose, uremie, bijnierinsufficiëntie, hyperparathyreoïdie en schildklieraandoeningen. Elektrolytafwijkingen, zoals hyponatriëmie, hypokaliëmie en hypercalciëmie, zijn ook bekende oorzaken. Minder vaak voorkomende oorzaken zijn paraneoplastische syndromen en hematologische aandoeningen, waaronder acute intermitterende porfyrie.
Medicamenteus geïnduceerde misselijkheid of braken komt veel voor, vooral binnen enkele dagen na start van de behandeling. Het begin van de symptomen kan sluipend zijn. Vaak betreffen het niet-steroïde ontstekingsremmende geneesmiddelen, antiaritmische middelen, antibiotica, anti-epileptica, opioïden en levodopa (zie ook tabel 2). Gebruik van opioïden kan leiden tot misselijkheid door gastroparese, centrale werking op chemoreceptor trigger zone en (zelden) invloed op evenwichtsorgaan. Overmatig en langdurig cannabisgebruik kan leiden tot het cannabinoïd hyperemesis syndroom. Medicijnen en toxinen leiden waarschijnlijk tot misselijkheid of braken door de chemoreceptor triggerzone te stimuleren [Sclocco 2016]. Daarnaast zijn chemotherapie en radiotherapie bekende oorzaken van misselijkheid en/of braken. Postoperatieve misselijkheid en/of braken treden meestal op binnen 24 uur na een chirurgische ingreep en kunnen worden veroorzaakt door anesthetica, opioïden of andere medicijnen.
Verschillende neurologische aandoeningen die gepaard gaan met verhoogde intracraniële druk, zoals hersentumoren, infectie, hydrocefalie, idiopathische intracraniële hypertensie en bloedingen, kunnen leiden tot braken, al dan niet gepaard met misselijkheid. Stoornissen van het evenwichtsorgaan zoals ziekte van Ménière, een vestibulair schwannoom of benigne paroxysmale positieduizeligheid kunnen eveneens misselijkheid en/of braken veroorzaken. Migraineaanvallen zijn vaak geassocieerd met misselijkheid en/of braken.
Ten slotte kunnen psychogene oorzaken ook een rol spelen bij misselijkheid en/of braken geïnduceerd door emotionele of fysieke stressoren. Deze aandoeningen kunnen bijvoorbeeld angst, depressie, anorexia nervosa en boulimia nervosa zijn.
Tabel 1 Oorzaken van misselijkheid en braken
| Categorie | Typen |
|---|---|
| Gastro-intestinaal |
Vertraagde maaglediging (gastroparese)
Mechanisch (obstructie of compressie van de maag, pylorus of duodenum) Gastritis, ulceratie
|
| Andere abdominale oorzaken | Obstipatie Ileus (mechanisch, paralytisch) Peritonitis carcinomatosa Levermetastasen Leverstuwing bij hartfalen Reflux Dumping syndroom na maagresectie Gastroenteritis, pancreatitis, cholecystitis, cholangitis, hepatitis, cystitis Galstenen, nierstenen Hoest of hik met reflectoir braken Radiotherapie, radiofrequency ablation (RFA) |
| Chemisch | Medicamenteus (zie ook tabel 2)
|
| Metabool | Electrolytstoornissen
Acute porfyrie |
| Neurologisch | Primaire en secundaire hersentumoren Leptomeningeale metastasen Meningitis
Epilepsie Totale schedelbestraling |
| Vestibulair | Medicamenteus
Tumor binnen/middenoor of schedelbasis |
| Psychogeen | Bepaalde geur- en smaakstoffen Hevige pijn Angst en spanning Depressie |
Medicatie of intoxicatie als oorzaak voor misselijkheid en/of braken (zie module Anamnese):
- Chemotherapie;
- Antiparkinsonmedicatie;
- Nicotine;
- Analgetica (aspirine, colchicine, NSAID, opioïden);
- Antibiotica, antivirale medicatie, tuberculostatica;
- Alcohol;
- Cardiovasculaire medicatie (anti-aritmica, beta-blokkers, calciumantagonisten, digoxine, diuretica);
- Cannabis;
- Gastrointestinale middelen (mesalazine, proton pompremmers, thiopurines)
- Hormonale preparaten (orale anticonceptiva, orale antidiabetica);
- Anti-epileptica;
- Vitaminepreparaten.
Impact van misselijkheid en braken
Misselijkheid kan een forse negatieve invloed hebben op de kwaliteit van leven van de patiënt. Dit is afhankelijk van de onderliggende oorzaak en beleving van de patiënt. Daarnaast hebben misselijkheid en braken impact op de kwaliteit van leven van de naasten, omdat misselijkheid en braken interfereert met sociale activiteiten zoals samen eten, koken, uitgaan. Dit is vaak een belangrijk sociaal-emotioneel aspect voor patiënt en naasten [Rhodes 2001, Bowers 2020, Lize 2020].
Chemotherapie geïnduceerde misselijkheid en braken leidt tot een afname van de kwaliteit van leven op fysieke en psychosociale domeinen in vergelijking met patiënten zonder misselijkheid en braken [Ballatori 2003].
Bowers M, Higginson IJ & Maddocks M (2024). Patient and carer experiences of cancer cachexia and its management.. Current Opinion in Supportive & Palliative Care, 18(3), 132-137.
Glare P, Miller J, Nikolova T, Tickoo R. Treating nausea and vomiting in palliative care: a review. Clin Intervent Aging 2011; 6: 243-59.
Harder S, Herrstedt J, Isaksen J et al. The nature of nausea: prevalence, etiology and treatment in patients with advanced cancer not receiving antineoplastic treatment. Support Care Cancer 2019; 27: 3071-80.
Hardy J, Davis MP. The management of nausea and vomiting not related to anticancer therapy in patient with cancer. Curr Treat Options Oncol 2021; 22: 17.
Lize N, Raijmakers N, van Lieshout R, Youssef-El Soud M, van Limpt A, van der Linden M & Beijer S (2020). Psychosocial consequences of a reduced ability to eat for patients with cancer and their informal caregivers: a qualitative study. European Journal of Oncology Nursing, 49.
Malec M, Shega JW. Management of Gastrointestinal Symptoms (Nausea, Anorexia and Cachexia, Constipation) in Advanced Illness. Med Clin North Am. 2020 May;104(3):439-454.
Mecadante S, Casuccio A, Fulfaro F. The course of symptom frequency and intensitiy in advanced cancer patient followed at home. J Pain Symptom Manag 2000; 21: 104-12.
Mosa ASM, Hossain AM, Lavoie BJ, Yoo I. Patient-related risk factors for chemotherapy-induced nausea and vomiting: a systemic review. Front Pharmacol 2020; 11; 329.
Rhodes VA, McDaniel RW. Nausea, vomiting, and retching: complex problems in palliative care. CA Cancer J Clin. 2001 Jul-Aug;51(4):232-48; quiz 249-52.
Roila F, Tonato M, Basurto C, et al.: Antiemetic activity of high doses of metoclopramide combined with methylprednisolone versus metoclopramide alone in cisplatin-treated cancer patients: a randomized double-blind trial of the Italian Oncology Group for Clinical Research. J Clin Oncol 1987; 5: 141-9.
Singh P, Yoon SS, Kuo B. Nausea: a review of pathophysiology and therapeutics. Ther Adv gastroenterol 2016; 9: 98-112.
Sclocco R, Kim J, Garcia RG, et al. Brain circuitry supporting mutliorgan autonomic outflow in response to nausea. Cereb Cortex 2016; 26: 485-97.
Solona JP, Gomes B, Higginson IJ. A comparison of symptom prevalence in far advanced cancer, AIDS, heart disease, chronic obstructive pulmonary disease and renal disease, J Pain Symptom Mange 2006; 31: 58-69.
Stephanson J, Davies A. An assessment of etiology-based guidelines for the management of nausea and vomiting in patients with advanced cancer. Support Care Cancer 2006; 14: 348-53.
Stern RM, Koch KL, Andrews PL. Nausea: mechanism and treatment. New York: Oxford Press; 2011.
Sullivan JR, Leyden MJ, Bell R: Decreased cisplatin-induced nausea and vomiting with chronic alcohol ingestion. N Engl J Med 1983; 309: 796.
Tonato M, Roila F, Del Favero A: Methodology of antiemetic trials: a review. Ann Oncol 1991; 2: 107-14.
Yee C, Drost L, Zhang L, Wan BA, Ganesh V, Tsao M, Barnes E, Pasetka M, DeAngelis C, Chow E. Impact of radiation-induced nausea and vomiting on quality of life. Support Care Cancer 2018; 26: 3959-66.

.png?lang=nl-NL)